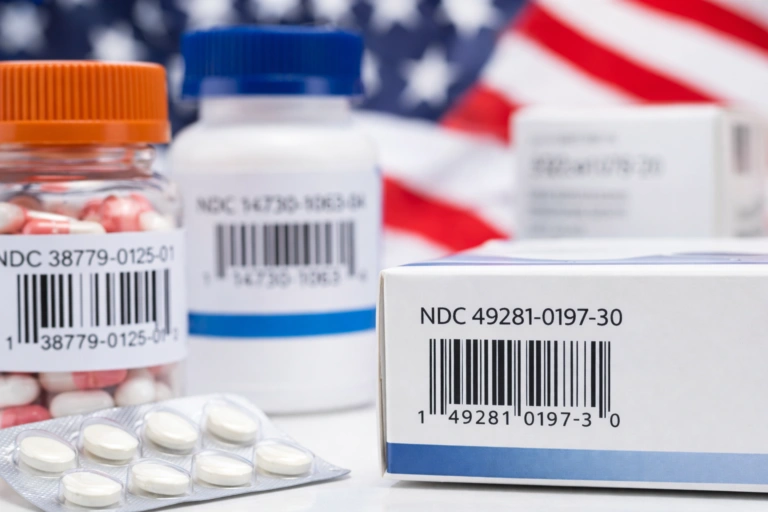
Egipski mandat dotyczący identyfikowalności produktów farmaceutycznych wymaga, aby każdy produkt leczniczy wprowadzany na rynek egipski posiadał unikalny identyfikator seryjny. Firmy, które nie są przygotowane operacyjnie, ryzykują opóźnienia w wysyłce, odrzucenie produktu, narażenie na zgodność z przepisami i zakłócenie dostępu do rynku.
Zrozumienie wymagań technicznych i operacyjnych Egipt farmacja serializacja zgodność, EDA ścieżka i ślad regulamin, oraz Egipt GS1 serializacja standardy ma obecnie zasadnicze znaczenie dla producentów, MAH, CMO i zespołów łańcucha dostaw działających w regionie.
Egipt pfarmaceutyczny serializacja
rymagania
EDA serializacja rymagania dla pfarmaceutyczny pprodukty
Egipskimi ramami identyfikowalności produktów farmaceutycznych zarządza Egipski Urząd ds. Leków (EDA).
EDA wymaga, aby każde nadające się do sprzedaży opakowanie farmaceutyczne zawierało Matryca danych 2D zgodna z GS1 kod kreskowy zawierający cztery obowiązkowe elementy danych:
- GTIN (Global Trade Pozycja Liczba) - identyfikator produktu
- Serial Liczba - unikalny identyfikator alfanumeryczny na opakowanie
- Partia/Lot Liczba - numer referencyjny partii produkcyjnej
- Wygaśnięcie Data - sformatowany jako RRRR-MM-DDT zgodnie z wymaganiami specyficznymi dla EDA
Ramy te są zasadniczo zgodne z globalnymi zasadami serializacji GS1 i wykazują podobieństwa do unijnych wymogów FMD i DSCSA. Egipt wprowadza jednak kilka specyficznych dla rynku zasad związanych z formatowaniem, raportowaniem i onboardingiem, które wymagają dedykowanej oceny i lokalnego dostosowania.
Jak Egipt pharma tstojak i twyścig ssystem worki
Koniec zei Egipt tstojak i twyścig czgodność
Egipt prowadzi pełny farmaceutyczny ścieżka i ślad model, a nie tylko weryfikacja w punkcie sprzedaży.
Serializowane dane produktu muszą być zgłaszane do repozytorium EDA od momentu produkcji lub importu aż do wydania, przy czym wszystkie transfery nadzoru muszą być rejestrowane w całym łańcuchu dostaw.
Co ważne, numery seryjne są nie wydany przez EDA. Producenci są odpowiedzialni za generowanie globalnie unikalnych numerów seryjnych powiązanych z numerami GTIN wstępnie zarejestrowanymi w EDA przed importem lub wydaniem produktu.
Podstawowe wymagania operacyjne obejmują:
- Generowanie numerów seryjnych i drukowanie kodów 2D Data Matrix na liniach pakujących
- Agregowanie danych na poziomie opakowania do skrzyń i palet, jeśli jest to wymagane.
- Przesyłanie danych wzorcowych serializacji do repozytorium EDA
- Przesyłanie powiadomień o dostawie w ramach łańcucha dostaw
- Walidacja dostaw serializowanych na poziomie hurtowni i aptek
- Zgłaszanie zdarzeń wydania na etapie zaopatrzenia pacjenta
Egipt EPCIS i data exchange rymagania
CSV rraportowanie vs EPCIS iintegracja w Egipt
Jednym z najbardziej niezrozumianych obszarów Egipt serializacja zgodność to architektura wymiany danych.
Na obecnym etapie wdrażania EDA wymaga CSV-.oparty serializacja raportowanie. Chociaż EPCIS i łączność oparta na API są oczekiwane w przyszłych fazach, obecnie nie jest dostępna żadna integracja API produkcyjnego.
Jednocześnie interoperacyjność pozostaje jednym z największych wyzwań operacyjnych. Nawet jeśli producent jest gotowy do serializacji, łańcuch zgodności nie powiedzie się, jeśli egipscy dystrybutorzy, importerzy lub apteki nie będą w stanie prawidłowo wymieniać serializowanych danych.
Kluczowe oczekiwania techniczne obejmują:
- Obsługa struktur zdarzeń GS1 EPCIS 1.2 lub nowszych
- Możliwość generowania zdarzeń wysyłki i odbioru
- Łączność za pośrednictwem zatwierdzonych mechanizmów przesyłania CSV lub plików
- Wdrażanie partnerów handlowych wśród egipskich dystrybutorów
- Przepływy pracy obsługi wyjątków dla rozbieżności numerów seryjnych i brakujących zdarzeń
Największy Egipt serializacja czgodność risks
Operacyjny i data iintegralność risks w Egipt tstojak i twyścig
Największe zagrożenia dla zgodności w Egipcie rzadko są związane z fizycznymi liniami serializacji. Większość producentów eksportowych posiada już możliwości serializacji.
Prawdziwym wyzwaniem jest utrzymanie dane integralność w poprzek w pełny dostawa łańcuch.
Ryzyko krytyczne obejmuje:
Ukryty Dane i dane podstawowe Problemy
Numery GTIN i dane produktu zarejestrowane w GS1 Egypt muszą być zgodne:
- opakowanie fizyczne
- Rejestry EDA
- dane podstawowe serializacji
Nawet niewielkie niespójności mogą powodować błędy walidacji.
Gotowość partnera handlowego
Egipscy hurtownicy i dystrybutorzy różnią się znacznie pod względem dojrzałości technicznej, podczas gdy MAH pozostają odpowiedzialni za kompleksową zgodność.
Dzieło sztuki i Opakowanie Opóźnienia
Dodanie lub modyfikacja kodów 2D Data Matrix wymaga złożenia wniosków i zatwierdzenia, które należy zaplanować odpowiednio wcześnie.
Równoległy Import Ryzyko
Produkty serializowane na inne rynki mogą nie przejść weryfikacji EDA, jeśli nie zostaną prawidłowo zarejestrowane i zgłoszone w systemie egipskim.
Raportowanie Oś czasu Ograniczenia
Terminy raportowania EDA są mierzone w godzinach kalendarzowych, a nie w godzinach pracy, co wymaga ciągłego monitorowania operacyjnego i gotowości do przedłożenia przed nadejściem przesyłki.
Produkcja Data Wymagania
Wymogi dotyczące daty produkcji zostały również przywołane przez EDA w bezpośredniej komunikacji z importerami, chociaż szczegółowe formalne wytyczne nie zostały jeszcze w pełni włączone do oficjalnej dokumentacji publicznej.
Przestój i Wyjątek Zarządzanie
Producenci muszą utrzymywać udokumentowane procedury awaryjne dla scenariuszy wydania offline i odroczonego raportowania.
Budynek an Egipt pharma serializacja pprojekt ppan
Zalecane Egipt tstojak i twyścig iwdrożenie timeline
Skuteczny program serializacji Egiptu powinien obejmować cztery równoległe strumienie pracy:
- serializacja techniczna
- zarządzanie głównymi danymi regulacyjnymi
- raportowanie danych
- integracja partnerów handlowych
Zalecane ramy czasowe:
- 12-18 miesiące dla firm rozpoczynających serializację
- 6-9 miesiące dla organizacji już spełniających wymogi EU FMD lub DSCSA
Sugerowane Projekt Fazy
Faza 1 - Assessment
- Analiza luk w stosunku do wymagań EDA
- Ocena gotowości partnera handlowego
- Audyt danych podstawowych GS1 Egipt
Faza 2 - Projektowanie i Konfiguracja
- Konfiguracja platformy dla formatów raportowania Egiptu
- Aktualizacje grafiki i opakowań
- Planowanie integracji partnerów
Faza 3 - Testowanie
- Kompleksowe testowanie środowiska EDA
- Partner UAT
- Walidacja scenariusza wyjątku
Faza 4 - Uruchomienie i Hypercare
- Wdrożenie komercyjne
- Monitorowanie zgłoszeń
- Szybkie rozwiązywanie problemów i stabilizacja
Zaangażowanie doświadczonej firmy konsultingowej w zakresie serializacji farmaceutycznej na wczesnym etapie oceny znacznie zmniejsza ryzyko projektu, koszty działań naprawczych i opóźnienia we wdrażaniu.
Klucz takeaways na Egipt pharma twyścigowość czgodność
- Egipt wymaga serializacji farmaceutycznej zgodnej z GS1 z obowiązkowym etykietowaniem 2D Data Matrix
- Raportowanie oparte na CSV jest obecnie obowiązkowe, podczas gdy integracja EPCIS/API jest oczekiwana w przyszłych fazach.
- Gotowość partnerów handlowych pozostaje jednym z największych ryzyk operacyjnych
- Integralność danych i synchronizacja danych podstawowych mają krytyczne znaczenie dla pomyślnej zgodności z EDA
- Wymagania specyficzne dla Egiptu wymagają dedykowanej walidacji, nawet w przypadku firm już spełniających wymogi EU FMD lub DSCSA.
Wnioski
Egipskie ramy identyfikowalności farmaceutycznej szybko ewoluują w jeden z najbardziej wymagających operacyjnie ekosystemów serializacji w regionie.
Sukces zależy nie tylko od serializacji na poziomie pakietu, ale także od:
- dokładne dane podstawowe
- rzetelne raportowanie
- interoperacyjność partnerów
- ciągła gotowość operacyjna
Organizacje, które strategicznie i proaktywnie podchodzą do kwestii zgodności serializacji w Egipcie, znacznie ograniczą ryzyko wdrożenia i unikną kosztownych zakłóceń podczas wdrażania i komercjalizacji.